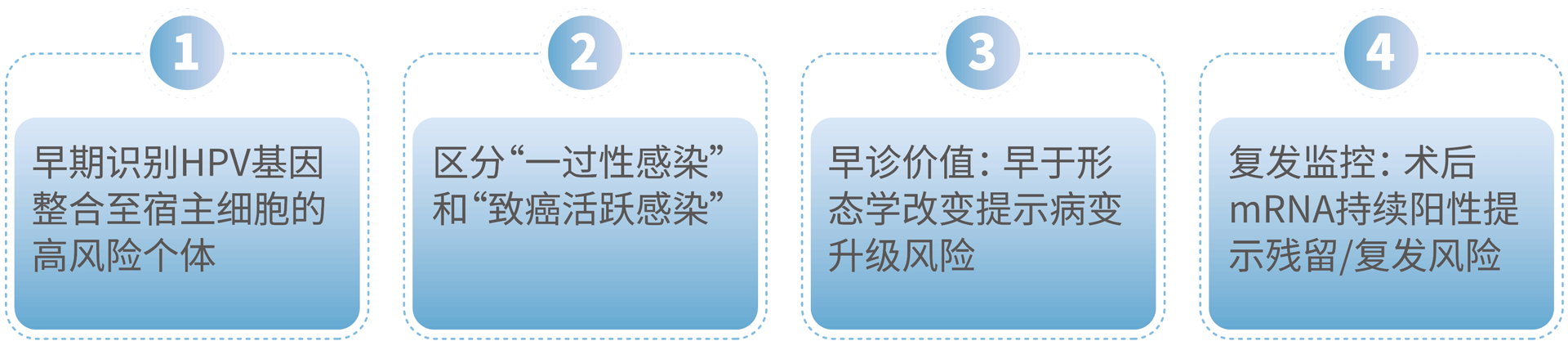
高危型HPV基因组整合至宿主细胞基因组是宫颈癌发生的关键早期分子事件,在宫颈上皮细胞恶性转化中起重要作用,为进展至侵袭性癌症的高风险指标。
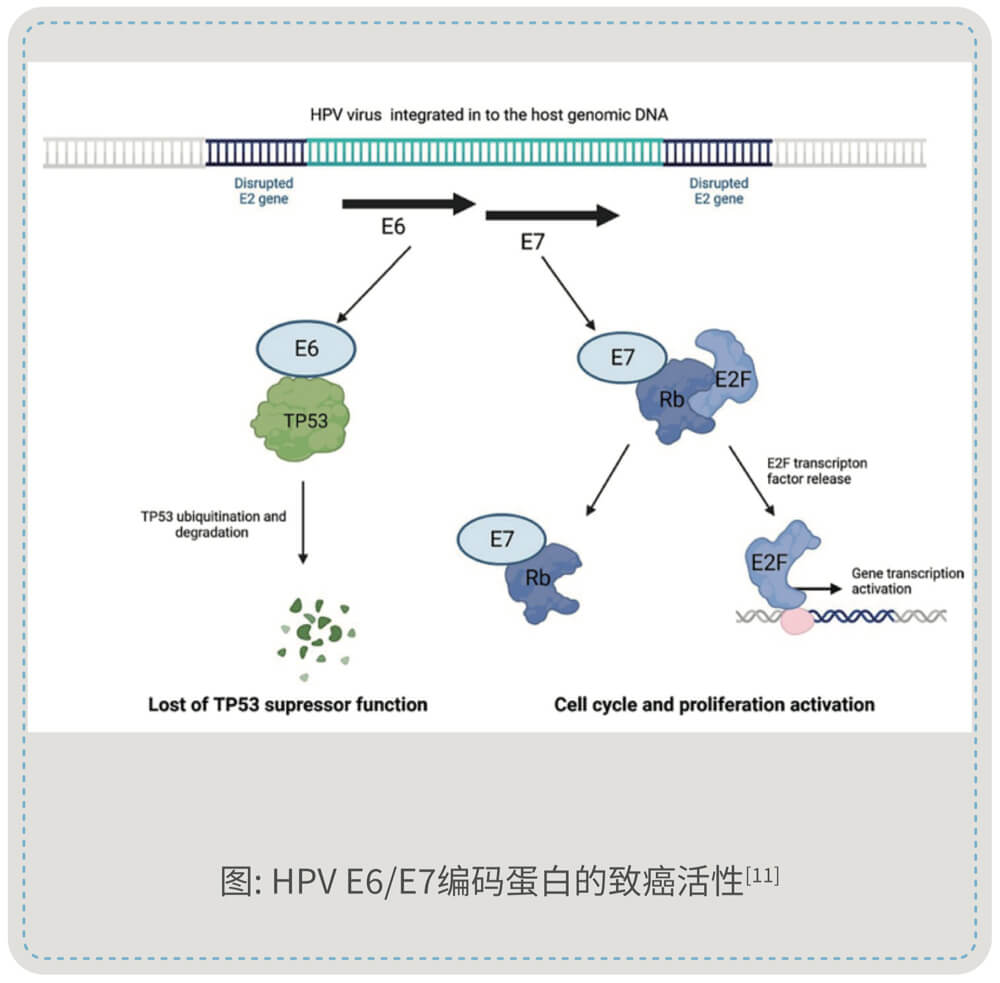
HPV基因整合过程中,E1/E2开放阅读框(open reading frame, ORF) 的缺失可能导致E2基因功能中断,进而导致E6/E7基因表达增强,促进E6/E7 mRNA大量转录并翻译为癌蛋白;E6蛋白可通过降解p53抑癌因子,E7蛋白通过失活pRb通路,协同破坏细胞周期调控,最终驱动细胞恶性转化。
因此E6/E7基因的持续性转录,即E6/E7 mRNA的稳定表达,是病毒整合入宿主基因组、由潜伏感染转为转化性感染的核心分子标志。
| 机构/会议/共识/组织 | 年份 | 核心推荐 |
|---|---|---|
| WHO宫颈癌前病变筛查和治疗指南(第二版) | 2021 | 建议由医护人员采集样本进行HPV mRNA检测,可作为初筛主要检测方法,可单独使用,也可结合分流策略进行,用于每5年定期筛查一次的人群 |
| ASCCP(美国阴道镜与宫颈病理学会)基于风险的宫颈癌筛查异常及癌前病变管理共识指南 | 2019 | 推荐高危型HPV DNA 和 mRNA 检测应根据其获批的筛查用途进行临床管理。 |
| SOGC(加拿大妇产科学会)HPV检测阳性管理指南及特定人群管理建议 | 2023 | HPV DNA 阳性且细胞学阴性者,E6/E7 mRNA 可用于分流,阴性者可无需立即转诊至阴道镜检查。 |
| HPV感染疾病相关问题专家共识(2017) | 2017 | 高危HPV DNA初筛阳性后可使用E6/E7 mRNA 检测进行分流,以指导阴道镜转诊及后续管理。 |
| 人乳头状瘤病毒核酸检测用于宫颈癌筛查中国专家共识(2022) | 2023 | 认可 E6/E7 mRNA 检测为HPV核酸检测常用方法学用于宫颈癌筛查。 |
RSCC™检测采用实时荧光定量PCR(qPCR) 技术,特异性靶向14种高危型HPV(包括16,18,31,33,35,39,45,51,52,56,58,59,66,68型)的E6/E7基因的mRNA。
检测到E6/E7 mRNA的存在,表明HPV病毒基因已开始转录,癌蛋白正在或即将被合成,提示病毒可能已经整合入人体基因组,细胞癌变风险显著增高。